Imagen: (a) estructura de interfaz y carga superficial en presencia de diferentes cationes; (b) la energía requerida para que ocurra la reacción de acoplamiento de CO bajo diferentes condiciones; (c)–(d) Correlaciones entre la capacidad catiónica, el volumen, la energía de solubilidad y la selectividad de los productos C2.
Escena más
Crédito: © Science China Press
en los últimos días, Revista Nacional de Ciencias Publicación de los resultados de la investigación del Prof. Jun Cheng (Universidad de Xiamen) y el Dr. Jiabo Lu (Instituto de Tecnología e Ingeniería de Materiales de Ningbo de la Academia de Ciencias de China). El equipo de investigación utilizó métodos de simulación de dinámica molecular ab initio para estudiar las propiedades microscópicas de la interfaz electroquímica y luego aplicó estos resultados para comprender el mecanismo detrás del efecto del catión en la selectividad de C.2 Productos en la reducción electrocatalítica de monóxido de carbono.
En muchas reacciones electrocatalíticas, los investigadores han descubierto que cambiar el catión por el electrolito puede ajustar significativamente la actividad y la selectividad catalíticas, pero todavía hay debate sobre el mecanismo microscópico involucrado en este proceso. Para abordar este problema, los investigadores utilizaron la reducción catalítica de monóxido de carbono como ejemplo y estudiaron sistemáticamente el efecto de diferentes cationes (incluidos varios iones de metales alcalinos e iones de alquilamonio) en la microestructura de Pt(111)-CO.anuncio/ interfaz solución acuosa, y su relación con la actividad de reacción de acoplamiento de dióxido de carbono. El estudio concluyó que: 1) La estructura de la capa de solubilidad del catión en la interfaz está relacionada con la energía iónica del agua. Iones con poca energía de hidratación, como el Cs+, es probable que se deshidraten en la interfase, coordinándose así con las moléculas de CO adsorbidas en la superficie e influyendo en la estabilidad de adsorción del CO y sus intermediarios de acoplamiento. 2) Las propiedades de los cationes afectan la capacitancia de la doble capa en la interfaz. En general, los iones con radios de agua más pequeños tienen una capacitancia de interfaz mayor, lo que puede explicar por qué la capacitancia de los iones de alquilamonio es menor que la de los iones de metales alcalinos. Además, los investigadores descubrieron dos fenómenos especiales en este trabajo: uno es el efecto de la clasificación excesiva de iones de agua de baja energía (como Cs+), lo que aumenta la capacitancia; La otra es que los iones de gran tamaño (como los iones de amonio propilo) reducen el contenido de agua en la interfaz, lo que reduce su capacidad de tamizado dieléctrico y reduce la capacitancia. 3) Los cálculos de la reacción de superficie encontraron que la energía de reacción de acoplamiento de dióxido de carbono en la superficie del electrodo está significativamente relacionada con la carga de la superficie, la coordinación de iones y los enlaces de hidrógeno con las moléculas de agua. Cuando se combina con el efecto de los cationes en las propiedades de la microestructura de la interfaz, la tendencia experimental de diferentes cationes en la selectividad electrorreductora de CO2 Los productos se pueden entender bien, Cs+~ t+ >k+ > yo+ Y yo4norte+ > Et4norte+ > relaciones públicas4norte+. Este trabajo proporciona una guía importante para el diseño de futuros sistemas de electrocatálisis CO/CO.
Ver artículo:
Comprensión molecular de los efectos de los cationes en la bicapa y su relevancia para la bicapa CO-CO
https://doi.org/10.1093/nsr/nwad105
revista
Revista Nacional de Ciencias
Descargo de responsabilidad: AAAS y Eurek Alert! No es responsable de la exactitud de los boletines enviados en EurekAlert! A través de organizaciones colaboradoras o por utilizar cualquier información a través del sistema EurekAlert.

«Alborotador. Amante de la cerveza. Total aficionado al alcohol. Sutilmente encantador adicto a los zombis. Ninja de twitter de toda la vida».



More Stories
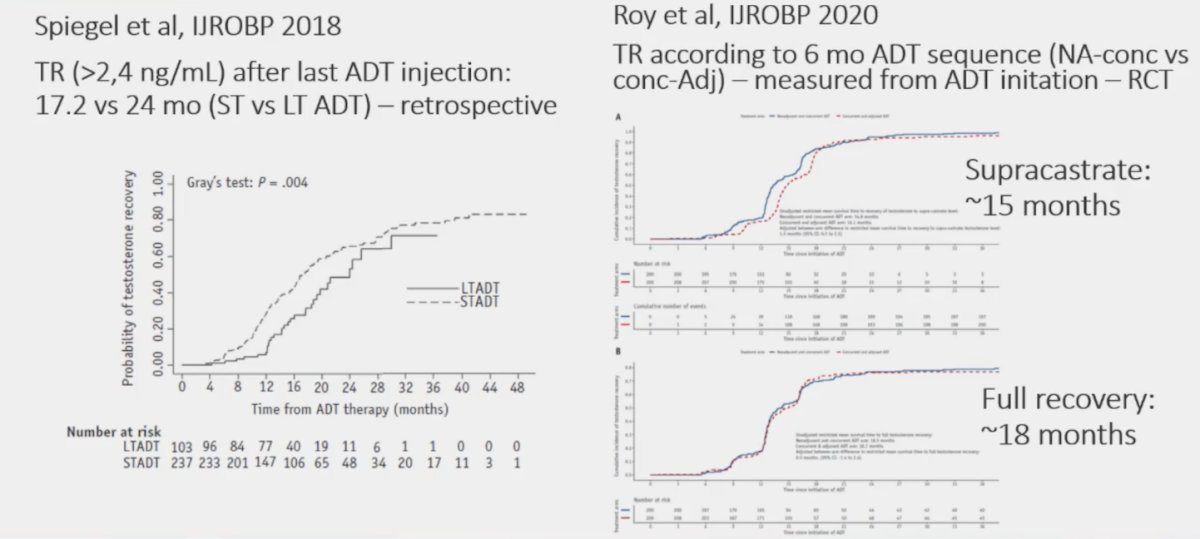
Restaurar la testosterona después de dejar el TDA: ¿quién corre el riesgo de no recuperarse a largo plazo?
Los científicos finalmente han descubierto signos de vida en un planeta dos veces más grande que la Tierra.
La niebla se encuentra con las montañas Salomón