(Noticias Nanwork) Las enzimas que escinden proteínas desempeñan un papel importante en muchos procesos fisiológicos. Estas proteasas generalmente existen en un estado inactivo y solo se activan bajo ciertas condiciones. Algunos están asociados con enfermedades como infecciones o cáncer, por lo que es importante contar con métodos que puedan detectar selectivamente proteasas activas.
en la revista angioandte chemi («Nanoestructuras plasmónicas codificadas por ADN para la detección de proteasas basada en actividad».), los científicos introdujeron una nueva clase de sensores de actividad de proteasa: nanopartículas de oro equipadas con ADN peptídico.
El equipo, dirigido por Devlina Samanta y Anna Capasso (Universidad de Texas en Austin, EE. UU.), demostró que estas nanosondas pueden detectar múltiples proteasas activas en paralelo (multiplexación). Este método funciona a temperatura ambiente y no requiere una preparación de muestras compleja ni instrumentación sofisticada.
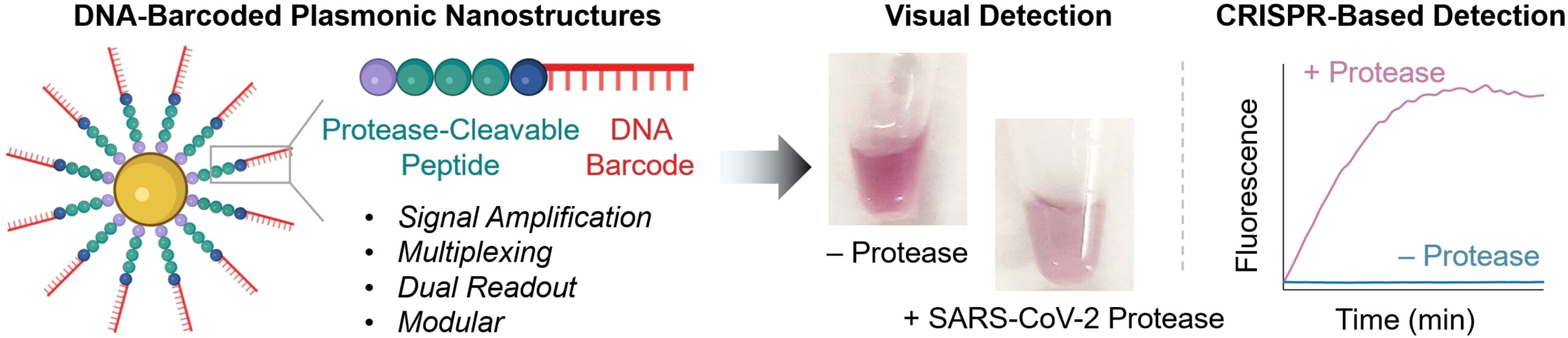
En el corazón de los nuevos sensores se encuentran nanopartículas de oro equipadas con cadenas formadas por péptidos y parte de ADN. La estructura del péptido está diseñada de tal manera que se escinde mediante detección de proteasas. El ADN actúa como un código de barras único para identificar el péptido y también amplifica la señal. Si la proteasa deseada está presente en su forma activa en la muestra, el péptido la escinde. Esto libera el código de barras de ADN en una solución, donde se puede detectar en función de su secuencia.
Para llevar a cabo este descubrimiento, el equipo utiliza un ensayo CRISPR/Cas12a: la enzima Cas12a se une a un ARN guía (ARNg) para formar un complejo inactivo. El ARNg contiene un segmento que se une específicamente al ADN del código de barras. Esto activa Cas12a, de modo que ahora puede «cortar» el ADN monocatenario (ssDNA). Para la prueba, los investigadores agregaron moléculas de ADN ss con el grupo de fluorescencia (fluoróforo) en un extremo y la unidad de extinción, que «apaga» la fluorescencia (siempre que esté lo suficientemente cerca), en el otro extremo. Si se corta el ssDNA, el fluoróforo y el extintor se alejan uno del otro. Esto da como resultado una fuerte fluorescencia que indica la presencia de la proteasa que se está probando (límite de detección de aproximadamente 58 pM).
Si no se dispone de instrumentos in situ y la prueba debe realizarse rápidamente, la detección es posible a simple vista: si la proteasa divide el péptido en la sonda, la carga superficial de las nanopartículas de oro cambia y se agregan. El color de las llamadas «nanoestructuras plasmónicas» depende en gran medida del grado de agregación. Es posible detectar concentraciones de proteasa nanomolar basándose en el cambio de color en la solución de prueba.
La detección múltiple de la proteasa 3CL y caspasa3 permitió al equipo demostrar la alta sensibilidad y selectividad de su nuevo método. 3CL es un marcador de infección activa por coronavirus y los pacientes con coronavirus a menudo también tienen una actividad elevada del marcador de apoptosis caspasa3. El potencial clínico de esta prueba también quedó demostrado por la detección de catepsina B, una proteasa asociada con el cáncer colorrectal, en tres líneas celulares cancerosas diferentes obtenidas de pacientes.
Estos nanotubos producen señales de fluorescencia 100 veces mayores en comparación con los sensores de proteasa comerciales basados en fluorescencia. Además, casi cualquier proteasa puede detectarse si se conoce el péptido que escinde. Combinadas, estas nanosondas pueden permitir la detección temprana de enfermedades y mejorar la precisión y confiabilidad de las pruebas de diagnóstico mediante la multiplexación.

«Alborotador. Amante de la cerveza. Total aficionado al alcohol. Sutilmente encantador adicto a los zombis. Ninja de twitter de toda la vida».



More Stories
El calor del manto renovó la corteza terrestre hace 3 mil millones de años
El primer fractal molecular regular de la naturaleza. investigación
Biogun es un colorido Metroidvania con una divertida historia sobre perros, vacunas… y tocino